La fibroina rappresenta il principale componente strutturale della seta naturale prodotta dal baco Bombyx mori ed è una delle proteine fibrose più studiate nel campo dei biomateriali naturali. All’interno della fibra di seta grezza essa costituisce mediamente tra il 70% e l’80% della composizione proteica, mentre la restante frazione è rappresentata prevalentemente dalla sericina, una proteina adesiva che riveste e cementa i filamenti di fibroina durante la formazione del bozzolo.
Dal punto di vista biochimico la fibroina appartiene alla categoria delle scleroproteine, ovvero proteine strutturali caratterizzate da elevata stabilità, insolubilità e resistenza meccanica. Queste caratteristiche consentono alla seta di possedere proprietà fisiche straordinarie che combinano resistenza alla trazione, elasticità e leggerezza, rendendo questo materiale biologico uno dei più performanti presenti in natura.
L’interesse scientifico verso la fibroina è cresciuto significativamente negli ultimi anni, soprattutto in relazione alle sue proprietà biologiche e alla sua versatilità come biomateriale. La combinazione di biocompatibilità, biodegradabilità e capacità di auto-organizzazione molecolare ha reso questa proteina oggetto di numerose ricerche nel campo delle biotecnologie, della medicina rigenerativa e dei materiali avanzati.
Struttura molecolare
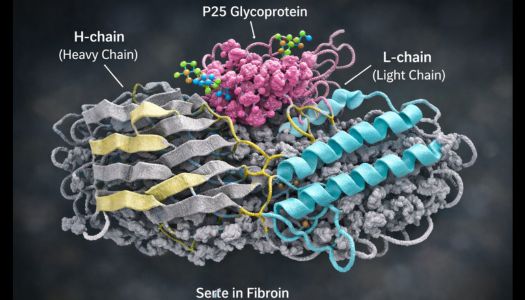
La fibroina della seta possiede una struttura molecolare altamente organizzata che contribuisce in modo determinante alle sue proprietà meccaniche e funzionali. La proteina è costituita principalmente da una catena pesante (Heavy Chain) e da una catena leggera (Light Chain) unite tramite un ponte disolfuro. A questo complesso si associa una glicoproteina denominata P25, che contribuisce alla stabilizzazione dell’assemblaggio proteico durante la formazione della fibra.
La catena pesante rappresenta la componente dominante della proteina e presenta una massa molecolare di circa 350 kDa. Dal punto di vista della sequenza amminoacidica essa è caratterizzata da una struttura altamente ripetitiva dominata dalla presenza di glicina, alanina e serina, amminoacidi che favoriscono la formazione di domini strutturali altamente ordinati.
Queste sequenze ripetitive si organizzano frequentemente secondo motivi del tipo Gly–Ala–Gly–Ala–Gly–Ser, che favoriscono la formazione di strutture secondarie a foglietto β antiparallelo. All’interno della fibra, tali strutture si impacchettano formando domini cristallini estremamente compatti.
La fibroina presenta inoltre una struttura gerarchica caratterizzata dall’alternanza tra regioni cristalline altamente ordinate e regioni amorfe più flessibili. Le prime conferiscono al materiale una notevole resistenza meccanica, mentre le seconde permettono una certa elasticità e capacità di deformazione. Questa combinazione di rigidità e flessibilità è alla base delle straordinarie proprietà meccaniche della seta e rappresenta uno degli esempi più sofisticati di ingegneria strutturale presente nei materiali biologici.
Proprietà fisico-chimiche della proteina della seta
Dal punto di vista fisico-chimico è una proteina intrinsecamente insolubile nella maggior parte dei solventi convenzionali, come acqua, etanolo ed etere. Può però anche essere solubilizzata mediante specifici sistemi solventi, come soluzioni saline concentrate o agenti caotropici, che consentono la dissociazione delle strutture secondarie e la successiva rielaborazione della proteina.
Una delle sue caratteristiche più rilevanti è la natura anfifilica, derivante dall’alternanza di domini idrofobici e idrofili lungo la catena polipeptidica. Questa proprietà consente alla proteina di auto-organizzarsi spontaneamente in strutture supramolecolari stabili e di essere trasformata in differenti morfologie materiali.
Attraverso specifiche tecniche di lavorazione, la fibroina può essere riorganizzata in numerose architetture strutturali, tra cui film sottili, idrogel, nanofibre, microsfere e scaffold tridimensionali. Tali strutture possono essere ottenute mediante processi come electrospinning, liofilizzazione, separazione di fase o auto-assemblaggio molecolare, dimostrando l’elevata versatilità tecnologica di questa proteina.
Dal punto di vista biologico, la fibroina presenta inoltre una notevole compatibilità con i tessuti viventi. Durante determinati processi di lavorazione possono emergere sequenze peptidiche bioattive in grado di favorire l’adesione cellulare attraverso interazioni con specifiche integrine presenti sulla superficie delle cellule. Questo comportamento facilita l’interazione tra biomateriale e sistema biologico, rendendo la fibroina particolarmente interessante per applicazioni biomedicali.
Un ulteriore elemento di interesse riguarda la biodegradabilità controllata della proteina. La fibroina può essere degradata da enzimi proteolitici presenti nell’organismo e la velocità di degradazione dipende principalmente dal grado di cristallinità del materiale. Strutture con maggiore organizzazione cristallina tendono a degradarsi più lentamente, mentre configurazioni più amorfe risultano più facilmente riassorbibili.
Fibroina come biomateriale avanzato
Le proprietà strutturali e biologiche di questa proteina hanno portato alla sua crescente considerazione come biomateriale di riferimento in diversi ambiti della ricerca scientifica. La combinazione di resistenza meccanica, stabilità strutturale e compatibilità biologica rende questa proteina particolarmente adatta allo sviluppo di materiali destinati all’interazione con sistemi biologici complessi.
Nel campo dell’ingegneria dei tessuti viene utilizzata per la realizzazione di scaffold tridimensionali che imitano l’architettura della matrice extracellulare. Queste strutture fungono da supporto per l’adesione, la proliferazione e la differenziazione cellulare, favorendo la formazione di nuovi tessuti.
E’ inoltre oggetto di studio per lo sviluppo di sistemi di rilascio controllato di farmaci, nei quali la struttura della fibroina può essere utilizzata per incapsulare molecole terapeutiche e rilasciarle progressivamente nel tempo. Questo approccio consente di modulare la cinetica di rilascio dei principi attivi e migliorare l’efficacia dei trattamenti farmacologici.
Un ulteriore ambito di applicazione riguarda i materiali destinati alla rigenerazione cutanea, dove la fibroina viene studiata per la produzione di medicazioni avanzate e supporti bioattivi in grado di favorire i processi di riparazione tissutale. La capacità della proteina di supportare la proliferazione cellulare e di interagire con la matrice extracellulare rappresenta un elemento chiave in queste applicazioni.
Parallelamente, le tecnologie di ingegneria genetica stanno aprendo nuove prospettive nello sviluppo di fibroine modificate contenenti sequenze bioattive specifiche. Attraverso tecniche di DNA ricombinante è infatti possibile integrare peptidi funzionali, fattori di crescita o molecole antimicrobiche direttamente nella struttura proteica, ampliando ulteriormente il potenziale applicativo di questo biomateriale.